 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知298K时,将反应Fe+2Fe3+=3Fe2+组成原电池,已知标准电极电势(Fe3+/Fe2+)=0.771V和(Fe2+/Fe)=-0.440V,则下列说法错误的是()。
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.电对Fe3+/Fe2+做正极
B.反应Fe+2Fe3+=3Fe2+的平衡常数大约为8×1040
C.电池组成式为(-)Fe|Fe2+(c1)||Fe2+(c2),Fe3+(c3)|Pt()
D.电池的标准电动势为0.331V
 答案
答案
 更多“已知298K时,将反应Fe+2Fe3+=3Fe2+组成原电池,已知标准电极电势(Fe3+/Fe2+)=0.771V和(Fe2+/Fe)=-0.440V,则下列说法错误的是()。”相关的问题
更多“已知298K时,将反应Fe+2Fe3+=3Fe2+组成原电池,已知标准电极电势(Fe3+/Fe2+)=0.771V和(Fe2+/Fe)=-0.440V,则下列说法错误的是()。”相关的问题
第1题
4-)=0.08mol·dm-1的高锰酸钾溶液20cm3在100kPa和298K混合使之反应,用热量计测得的热量为-1200J。该反应的计量方程可用下面两种写法表示,分别求出相应的ξ 和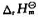 (298K) ;
(298K) ;
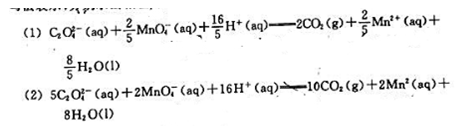
第2题
第3题
已知



(A) 减少 (B) 增大
(C) 不变 (D) 可能减小,也可能增大
第4题
在一渗析膜左侧将1.3×10-3kg盐基胶体(RH)溶于0.100dm3的极稀盐酸中,胶体酸完全解离。渗析膜右侧置1.0×10-4m3纯水。298K时达平衡后测得左侧、右侧的pH值分别为2.67和3.26,求胶体酸的摩尔质量。
第5题
今有含SO2的空气需要净化处理。采用以活性炭为催化剂,以水为液体介质的滴流床反应器,在0.101MPa,25℃下将SO2氧化为SO3,溶于水而成稀硫酸从反应器底部流出。反应的控制步骤是O2在催化剂表面的吸附,以O2表示的反应速率
rA=ηρPkcAS[mol/(cm3·s)](按床层体积计)
式中,cAS为催化剂表面处的O2浓度,单位为mol/cm3。已知:内扩散有效因子η=0.6,堆密度ρb=1.0g/cm3,1级反应速率常数k=0.06cm3/(g·s),床层空隙率ε=0.3,kLSaS=0.3s-1,kLaL=0.03s-1,气体流量为100cm3/s,O2在水中溶解度的亨利常数H=5.0,反应器直径10cm,塔顶入口处气体的摩尔分数分别为SO22%,O219%,N279%。试求SO2转化率为80%时滴流床反应器的床层高度。
第6题
已知可逆反应: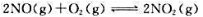 在298.15K下进时的
在298.15K下进时的 计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中
计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中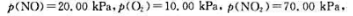 判断反应进行方向。
判断反应进行方向。
第7题
用钢管将压力为0.32MPa(表压)、温度为298K、流量为0.35Nm3/s的天然气(以100%甲烷计)送往150m(包括局部阻力的当量长度)外的燃烧喷嘴,要求进喷嘴前燃气的压力不低于0.07MPa(表压)。设流动为等温,天然气的平均摩尔质量为16kg/kmol,黏度为1.0×10-5Pa.s,大气压为0.10MPa。试求输送管道的直径。
第10题
298K时测得不同浓度c下氢化肉桂酸水溶液的表面张力σ的数据如下表所示:
 求浓度为0.0041kg/kg及0.0050kg/kg时溶液表面吸附量
求浓度为0.0041kg/kg及0.0050kg/kg时溶液表面吸附量
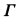 。
。
第11题
有一复合反应

已知:cA0=1kmol/m3,k1=10e(-3500/T),k2=1012e(-10500/T),k3=103e(-7000/T),操作温度在280K~350K范围。
求:(1)每molA可获得最大S的量;
(2)求生成99%cS,最大时的最小停留时间;
(3)若k1变为k1=107e(-3500T),其他不变,重复(2)的计算。