 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298.15K时将5.2589g固体NHHS样品放入一3.00L的真空容器中,经过足够时间后建立平衡,NH4HS(
s)=H3(g)+H2S(g).容器内的总压是66.7kPa,一些固体,NH4HS保留在容器中.计算:(1)298.15K时的K值;(2)固体,NH4HS的分解率;(3)如果容器体积减半,容器中周体,NH4HS物质的量如何变化?
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
s)=H3(g)+H2S(g).容器内的总压是66.7kPa,一些固体,NH4HS保留在容器中.计算:(1)298.15K时的K值;(2)固体,NH4HS的分解率;(3)如果容器体积减半,容器中周体,NH4HS物质的量如何变化?
 答案
答案
 更多“298.15K时将5.2589g固体NHHS样品放入一3.00L的真空容器中,经过足够时间后建立平衡,NH4HS(”相关的问题
更多“298.15K时将5.2589g固体NHHS样品放入一3.00L的真空容器中,经过足够时间后建立平衡,NH4HS(”相关的问题
第2题
已知可逆反应: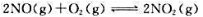 在298.15K下进时的
在298.15K下进时的 计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中
计算该可逆反应的标准平衡常数。在298.15K时,当反应系统中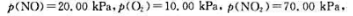 判断反应进行方向。
判断反应进行方向。
第3题
第4题
在1.5mol·L-1A溶液中加入一定量B,在298.15K时发生反应: 当反应达到平衡时.
当反应达到平衡时.
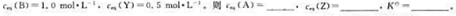
第5题
A.-195kJ·mol-1
B.195kJ·mol-1
C.-875kJ·mol-1
D.875kJ·mol-1
第6题
已知下列可逆反应: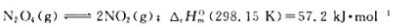 利用有关物质的热力学数据,计算此可逆反应在298.15K和350.15K时的标准平衡常数。
利用有关物质的热力学数据,计算此可逆反应在298.15K和350.15K时的标准平衡常数。
第7题
A.193kJ·mol-1
B.873kJ·mol-1
C.-193kJ·mol-1
D.-873kJ·mol-1
第8题
KCl(s)298.15K时的溶解过程: KCl(s)==K+(aq,ao)+Cl-(aq,∞)△Hm=17.1810/mol已知Cl-(aq,∞)和KCl(s)的摩尔生成焓分别为一167.4410/mol和一435.87kJ/mol,求K+(aq,∞)的摩尔生成焓。
第9题
298.15K时,Mg(OH)2的标准溶度积常数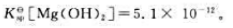 试计算:
试计算:
(1)Mg(OH)2在水中的溶解度:
(2)Mg(OH)2饱和溶液中的Mg2+、OH-的浓度和溶液的pH;
(3)Mg(OH)2在0.010mol·L-1NaOH溶液中的溶解度;
(4)Mg(OH)2在0.010mol·L-1MgCl2溶液中的溶解度。
第11题
A.取用腐蚀和刺激性药品时,尽可能带上橡皮手套和防护眼镜
B.倾倒时,切勿直对容器口俯视;吸取时,应该使用橡皮球
C.多取的试剂可倒回原瓶,避免浪费
D.瓶塞应倒置桌面上,以免弄脏,取用试剂后,立即盖严,将试剂瓶放回原处,标签朝外
E.要用干净的药匙取固体试剂,用过的药匙要洗净擦干才能再用
F.开启有毒气体容器时应带防毒用具