 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据分子轨道理论,O2分子中的化学键为()。
A、1个σ键
B、2个三电子π键
C、1个σ键和1个π键
D、1个σ键和2个三电子π键
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、1个σ键
B、2个三电子π键
C、1个σ键和1个π键
D、1个σ键和2个三电子π键
 答案
答案
 更多“根据分子轨道理论,O2分子中的化学键为()。”相关的问题
更多“根据分子轨道理论,O2分子中的化学键为()。”相关的问题
第1题
A.原子轨道的杂化,只有在形成分子的过程中才会发生,而孤立的原子是不可能发生杂化的
B.只有能量相近的原子轨道才能发生杂化
C.一定数目的原子轨道杂化后,可以得到更多数量的杂化轨道
D.CH4分子中有四个能量相等的C—H键,键角为109°28′,分子的空间构型为正四面体,这一情况可以用杂化轨道理论解释
第2题
试指出石墨层状分子中碳原子数与C—C化学键(将每对邻近的碳原子与碳原子间的连线看作一个化学键)的相对比例。
第7题
A、酸碱反应的实质是质子的转移反应
B、酸只能是中性分子
C、在共酸碱HA-A水溶液中,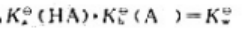
D、酸越强,则其共轭碱就越弱
第10题
将下列大气层的影响情况一一对应。
1).大气的吸收作用
A、各种气体分子、水分子(云雾)、尘埃等
B、氧(O2)、臭氧(O3)和水气(H2O)
C、云层反射
2).大气的散射作用
A、各种气体分子、水分子(云雾)、尘埃等
B、氧(O2)、臭氧(O3)和水气(H2O)
C、云层反射
3).大气的反射作用
A、各种气体分子、水分子(云雾)、尘埃等
B、氧(O2)、臭氧(O3)和水气(H2O)
C、云层反射