 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取只含FeCl3和AlCl3的混合物的质量5.9600g,两种氯化物转变成水合氧化物后,灼烧得到Fe2O3和Al2O3的混合氧
称取只含FeCl3和AlCl3的混合物的质量5.9600g,两种氯化物转变成水合氧化物后,灼烧得到Fe2O3和Al2O3的混合氧化物的质量为2.6300g,计算原混合物中Fe和Al的含量。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取只含FeCl3和AlCl3的混合物的质量5.9600g,两种氯化物转变成水合氧化物后,灼烧得到Fe2O3和Al2O3的混合氧化物的质量为2.6300g,计算原混合物中Fe和Al的含量。
 答案
答案
 更多“称取只含FeCl3和AlCl3的混合物的质量5.9600g,两种氯化物转变成水合氧化物后,灼烧得到Fe2O3和Al2O3的混合氧”相关的问题
更多“称取只含FeCl3和AlCl3的混合物的质量5.9600g,两种氯化物转变成水合氧化物后,灼烧得到Fe2O3和Al2O3的混合氧”相关的问题
第1题
无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上由铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按以下图所示流程进行一系列反应来制备无水AlCl3。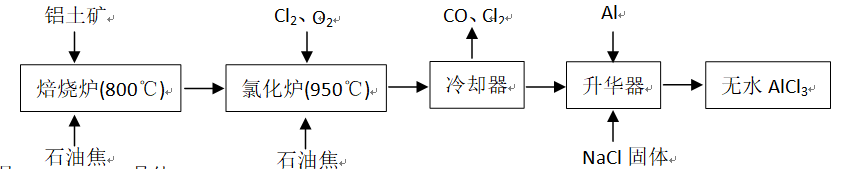
问题一、AlCl3是()晶体。
问题二、氯化炉中Al2O3、C12和C反应的化学方程式是()。
问题三、冷却器排出的尾气中含有大量CO和少量Cl2,需用Na2SO3溶液除去Cl2,写出此反应的离子方程式是()。
问题四、升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是()。
问题五、为测定无水AlCl3产品的纯度,现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.32g。则AlCl3产品的纯度为()。
第3题
称取0.1325g含ZrO2和HfO2并含其他杂质的混合物样品,用适当方法将ZrO2和HfO2同时与混合物中的其他杂质分离开后,再称重得ZrO2和HfO2共0.1194g。再将所得氧化物溶解,配制成100.00mL金属离子溶液。取25.00mL此溶液,用0.01000mol·L-1EDTA溶液滴定,用去21.67mL,求样品中ZrO2和HfO2的质量分数。已知ZrO2和HfO2的相对分子质量分别为123.2和210.5。
第4题
有一黄色结晶(Ⅰ),HCl-Mg反应显红色,Molisch反应(),FeCl3反应(),ZrOCl2反应呈黄色,但加入枸橼酸后黄色褪去。IR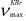 max(KBr)cm-1:3520,3470,1660,1600,1510,1270,1100~1000,840。Ⅰ的UVλnm如下:
max(KBr)cm-1:3520,3470,1660,1600,1510,1270,1100~1000,840。Ⅰ的UVλnm如下:
CH3OH 252,267(sh),346;
NaOMe 261,399;
AlCl3272,426;
AlCl3/HCl 260,274,357,385;
NaOAc 254,400;
NaOAc/H3BO3256,378。
Ⅰ的1H-NMR(DMSO-d6,TMS)δ:7.20(1H,d,J=3Hz);6.92(1H,dd,J=8Hz,3Hz);6.70(1H,d,J=8Hz);6.62(1H,d,J=2Hz);6.43(1H,d,J=2Hz);6.38(1H,s);5.05(1H,d,J=7Hz),其余略。
Ⅰ酸水解后检出D-glc和苷元,苷元的分子式为C15H10O6。FAB-MS示分子中含一分子葡萄糖。试回答下列各问:

第6题
A.混合物X中必定含有Na2CO3,不含Al2(SO4)3
B.溶液Z中溶质主要是钠盐,且必含NaHCO3
C.灼烧沉淀Y,可以得到黑色物质
D.往溶液Z中加入Cu粉,若不溶解,说明X中不含FeCl3
第8题
A.只含Fe2+
B.含Cu2+和Fe2+
C.含Cu2+和Fe3+
D.只含Fe3+
第9题
A.用焰色反应区别K2SO4和K2CO3
B.用酚酞溶液检验某溶液是否呈酸性
C.通入Cl2除去FeCl3溶液中的FeCl2
D.加入Fe粉除去AlCl3溶液中的杂质CuCl2